VIDEOCAST
08/04/2024: Insuficiència cardíaca avançada
VIDEOCAST
04/03/2024: Implant percutani de vàlvula aòrtica (TAVI) a Catalunya el 2023
VIDEOCAST
01/03/2024 Codi IAM a Catalunya: 15 anys d'èxit compartit
VIDEOCAST
31/01/2024 Noves eines per a la prevenció cardiovascular
VIDEOCAST
08/01/2024 Pactos por tu Corazón i Estenosis valvular aòrtica. ¿Què fer quan les dades no quadren?
VIDEOCAST
17/11/2023 Mort Sobtada
VIDEOCAST
09/11/2023 II Jornades Cardio-Onco-Hematologia
VIDEOCAST
06/11/2023 Diabetis i Cardiopatia
[AMPLIEM EL TERMINI] 02/04, data límit per sol·licitar una de les 2 beques
Es convoquen DUES beques per a projectes de recerca originals i inèdits. Cada beca està dotada amb 10.000 € més 1.000 € addicionals si el treball és acceptat per ser publicat en una revista amb Impact Factor. La data límit de recepció de les memòries és el 2 d'abril de 2024. Consulta les bases a: https://www.catcardio.cat/formacio/beques-i-premis
[AMPLIEM EL TERMINI] 26/03, data límit per enviar comunicacions
S'ha ampliat el termini per enviar comunicacions (orals o pòsters) pel 36è Congrés de la Societat Catalana de Cardiologia fins al 26 de març de 2024. Tota la informació i formulari: https://catcardiocongres.cat/index.php/abstracts
Descarrega't el calendari d'activitats del curs 2023/2024
Ja et pots descarregar el calendari d'activitats previstes per aquest nou curs 2023/2024 clicant sobre el títol de la notícia. És una forma de tenir una foto fixa de quines activitats s'organitzen des de la Societat Catalana de Cardiologia. Estigueu atents perquè l'anirem actualitzant. Si no veus el link de descàrrega, copia i enganxa aquest enllaç al teu navegador: https://bit.ly/3tW44cL
18 de març: data límit per enviar comunicacions pel 36è Congrés de la Societat Catalana de Cardiologia
Del 29 al 31 de maig la Societat Catalana de Cardiologia celebrarà el seu 36è Congrés. Per aquest motiu, ja es poden enviar les comunicacions que es volen presentar durant el congrés. Teniu temps fins el 18 de març. Trobareu tota la informació clicant en el títol de la notícia. #CatCardioCongres36
Ja s’han publicat les bases per a les 2 beques de la Societat.
Es convoquen DUES beques per a projectes de recerca originals i inèdits. Cada beca està dotada amb 10.000 € més 1.000 € addicionals si el treball és acceptat per ser publicat en una revista amb Impact Factor. La data límit de recepció de les memòries és el 30 de març de 2024. Consulta les bases a: https://www.catcardio.cat/formacio/beques-i-premis
L'Associació Catalana d’Hipercolesterolèmia Familiar (ASCAHIFA) comença a caminar
Un grup de pacients amb hipercolesterolèmia familiar han creat l’Associació Catalana d’Hipercolesterolèmia Familiar (ASCAHIFA). El seu objectiu principal és donar la màxima difusió de la hipercolesterolèmia familiar per tal de millorar l’accés al diagnòstic i al tractament precoç dels afectats per aquesta malaltia. Aquesta missió no la durant a terme sols, sinó que compten amb l’assessorament d’un comitè de professionals de la salut que els dona accés a informació relacionada amb nous fàrmacs, tractaments i recomanacions d’hàbits saludables d’estil de vida. Trobareu més informació a www.hipercolesterolemiafamiliar.org i a l’adreça de correu electrònic: ascahifa@gmail.com.
2a Jornada d'entrenament en habilitats tècniques per a residents de cardiologia 2023
La Societat Catalana de Cardiologia continua apostant un any més per la formació als residents en cardiologia del nostre territori. Novament, convoquem la 2a jornada d'entrenament en habilitats tècniques per als R3 de cardiologia de Catalunya, que es durà a terme el 9 de novembre de 2023, entre les 9 h i les 18 h, al Centre de Simulació Clínica Avançada de l’Hospital Vall d'Hebron (Barcelona).
Jornada d'entrenament en habilitats tècniques per a residents de cardiologia 2023
La Societat Catalana de Cardiologia continua apostant un any més per la formació als residents en cardiologia del nostre territori. Novament, convoquem la II jornada d'entrenament en habilitats tècniques per a residents de Cardiologia, que es durà a terme l’11 de maig de 2023, entre les 8:30 h i les 18:30 h, al Centre de Simulació Clínica Avançada de l’Hospital Vall d'Hebron (Barcelona). Cada taller tindrà una durada d’1,5 hores, en les quals els residents podran dur a terme i perfeccionar cada tècnica en models de simulació.
[AMPLIEM EL TERMINI] 10/04, data límit per la recepció de les memòries per a la convocatòria de 2 beques per a projectes de recerca 2023 de la Societat Catalana de Cardiologia
Es convoquen DUES beques per a projectes de recerca originals i inèdits. Cada beca està dotada amb 10.000 € més 1.000 € addicionals si el treball és acceptat per ser publicat en una revista amb Impact Factor. La data límit de recepció de les memòries és el 10 d'abril de 2023. Consulta les bases a: https://www.catcardio.cat/formacio/beques-i-premis
[AMPLIEM EL TERMINI] Data límit per enviar comunicacions pel 35è Congrés de la Societat Catalana de Cardiologia
S'ha ampliat el termini per enviar comunicacions (orals o pòsters) pel 35è Congrés de la Societat Catalana de Cardiologia fins al 20 de març de 2023. Es poden incloure fins a 9 autors, inclòs el primer signant. Tota la informació i formulari: https://catcardiocongres.cat/index.php/abstracts
El Dr. Artur Evangelista i Masip, president de la Societat Catalana de Cardiologia, rebrà la Medalla d'Or de l'Asociación de Imagen Cardiaca de la SEC
Durant el 41 Congrés de l'Associació que se celebrarà a Sevilla el 23-24 de febrer del 2023 s'entregarà la Medalla d'Or de l'Asociación de Imagen Cardiaca de la Sociedad Española de Cardiología (SEC) al Dr. Artur Evangelista i Masip, president de la Societat Catalana de Cardiologia. A l'acte, el Dr. Evangelista donarà la conferència magistral titulada "Una visió holística de la patologia aòrtica". Anteriorment, s'han donat dues medalles d'or prèviament, al Dr. Valentin Fuster i al Dr. Miguel Ángel García Fernández.
El 14 de març serà l'últim dia per enviar comunicacions pel 35è Congrés de la Societat Catalana de Cardiologia
Del 31 de maig al 2 de juny la Societat Catalana de Cardiologia celebrarà el seu 35è Congrés. Per aquest motiu, ja es poden enviar les comunicacions que es volen presentar durant el congrés. Teniu temps fins el 14 de març. Trobareu tota la informació clicant en el títol de la notícia. #CatCardioCongres35
Oberta la convocatòria de 2 beques per a projectes de recerca 2023 de la Societat Catalana de Cardiologia
Es convoquen DUES beques per a projectes de recerca originals i inèdits. Cada beca està dotada amb 10.000 € més 1.000 € addicionals si el treball és acceptat per ser publicat en una revista amb Impact Factor. La data límit de recepció de les memòries és el 30 de març de 2023. Consulta les bases a: https://www.catcardio.cat/formacio/beques-i-premis
2a Jornada d'entrenament en habilitats tècniques en cardiologia mitjançant simulació clínica per a residents de 3r any
Continuant amb la iniciativa de formació per a residents iniciada aquest any per la Societat Catalana de Cardiologia, el 16 de novembre es durà a terme la 2a jornada d'entrenament en habilitats tècniques en cardiologia mitjançant simulació clínica per a residents de 3r any. Es farà al Centre de Simulació Avançada de l’Hospital Vall d’Hebron i s’impartiran tallers de Toracocentesis i ecografia pulmonar, ventilació mecànica invasiva, monitorització hemodinàmica i ecocardiografia transesofàgica. La jornada és finançada per la SCC.
Rehabilitació cardíaca en línia després d’un infart o d’una angina de pit - La Societat Catalana de Cardiologia presentarà durant el seu congrés anual aquest innovador programa de rehabilitació Cardíaca.
El programa “Recupera’t” neix amb l'objectiu d'acompanyar i ajudar en el procés de recuperació de les persones que han tingut un infart de miocardi o una angina de pit. El programa és gratuït i consta de dues parts. D’una banda, una sèrie de vídeos pedagògics sobre tabac, alimentació, salut mental i control dels factors de risc per tal que el pacient sàpiga què l’hi ha passat i què ha de fer a partir d’aquell moment. I de l’altra, un programa d’entrenament físic penjat a la xarxa. La idea és que el pacient pugui realitzar el programa d’exercici físic no supervisat, amb l’autorització prèvia del metge referent que haurà de confirmar que és un pacient de baix risc i que pot fer esport des del seu domicili, amb seguretat. Un cop el metge hagi donat el vistiplau, el pacient podrà seguir els exercicis que es proposen en funció de l’edat i dels problemes osteomusculars. Aquests consells i exercicis es poden complementar amb 4 classes de ioga, ordenades segons el nivell de dificultat. La pràctica de ioga després d’un infart contribueix a millorar la qualitat de vida, ja que té efectes beneficiosos en l’estat de la forma física, el control de l'ansietat, la capacitat de concentració i en la millora de la qualitat de la son (insomni). “Recupera’t” ha estat ideat per un equip multidisciplinari de professionals que es dediquen a la Rehabilitació Cardíaca; i ha comptat amb el suport de la Societat Catalana de Cardiologia i del Pla Director de les Malalties Cardiovasculars del Departament de Salut. El programa s’ha desenvolupat com una eina innovadora i àgil. El pacient s’hi podrà connectar des de casa, des del primer dia de l’alta hospitalària; cosa que l’ajudarà a resoldre els dubtes que li puguin anar sorgint durant el procés de recuperació. Tots els professionals de la salut podran prescriure el programa “Recupera’t”. L’acte de presentació del programa “Recupera’t” tindrà lloc el proper 1 de juny a les 19h a l’aula Ramon y Cajal de la Universitat de Barcelona, la seu Central de la Gran Via de les Corts Catalanes, 585, Barcelona.
1a Jornada d'entrenament en habilitats tècniques per a redisents de Cardiologia
Aquesta primera jornada, que se celebrarà el 26 de maig de 2022 al Centre de Simulació Avançada de l’Hospital Vall d’Hebron, serà exclusivament per a R3 en cardiologia de Catalunya. Hi ha previstos dos dies de tallers, el dia 26 de maig s’impartiran tallers de Vies venoses centrals ecoguiades, Pericardiocentesis, Via aèria i Ventilació mecànica no invasiva. El segon dia, data que encara està per determinar, s’impartiran tallers: toracocentesi, Ventilació mecànica invasiva, Monitoratge hemodinàmica, ecocardiografia transesofàgica. Aquesta formació per a residents està íntegrament finançada per la SCC.
[S'HA AMPLIAT EL TERMINI] Oberta la convocatòria de beques de la Societat Catalana de Cardiologia 2022
[S'HA AMPLIAT EL TERMINI FINS EL DIA 3/04] S’han convocat 2 beques per a projectes de recerca originals i inèdits. Cada beca està dotada amb 10.000 € + 1.000 € addicionals si el treball és acceptat per ser publicat en una revista amb Impact Factor. La data límit de recepció de les memòries és el 3 d'abril de 2022. Les bases les trobareu a: https://www.catcardio.cat/formacio/beques-i-premis
L’embaràs és una oportunitat per a detectar a dones amb risc cardiovascular. El grup de treball interdisciplinari de la Societat Catalana de Ginecologia i Obstetrícia ha divulgat un document de consens sobre “Risc vascular a partir del 4t trimestre”.
Amb motiu del Dia Internacional de la Dona i el Dia Internacional del Risc cardiovascular que es commemoren els pròxims 8 i 14 de març, el grup de treball interdisciplinari de la Societat Catalana de Ginecologia i Obstetrícia ha divulgat un document de consens sobre “Risc vascular a partir del 4t trimestre”, amb l’objectiu de formar i conscienciar a tots els professionals implicats en el seguiment i tractament d’aquestes patologies desenvolupades durant l’embaràs i que comporten un risc vascular que perdura després del part. Es pot consultar la nota de premsa completa en aquest enllaç: http://lnxacademia.cat/files/204-9670-FITXER/Notapremsa14322.pdf Si vols consultar el cartell, pots fer-ho a: http://intranet.academia.cat/files/204-9675-FITXER/POSTERINFORMATIVOv14.03.22.jpg
El XXXIV Congrés de la Societat Catalana de Cardiologia se celebrarà de l’1 al 3 de juny a la Universitat de Barcelona.
El comitè organitzador del Congrés de la Societat Catalana de Cardiologia ha anunciat que després de dos anys de congrés en format virtual, el 34è Congrés serà altra vegada presencial i se celebrarà els dies 1-3 de juny de 2022 a la Universitat de Barcelona, a la seu central de Plaça Universitat. El Comitè desitja que el congrés sigui molt participatiu i permeti el retrobament de la majoria de cardiòlegs, infermeres i altres especialistes vinculats a la patologia cardiovascular a Catalunya. Ja està disponible la web del Congrés amb més informació a: www.catcardiocongres.cat | Pots seguir totes les novetats del congrés amb el hashtag #CatCardioCongres34
#CatCardioCongres33. El 15 de setembre a les 13:30 hores s’inaugura el 33è Congrés virtual de la Societat Catalana de Cardiologia.
El 15 de setembre a les 13:30 hores s’inaugura el 33è Congrés virtual de la Societat Catalana de Cardiologia, seran 3 dies plens d’activitats que es podran seguir a Twitter amb el hashtag #CatCardioCongres33. Durant la clausura del Congrés, el divendres 17 a les 20:30 hores, es concediran els premis a les millors comunicacions, i es farà públic els guanyadors/es de les dues Beques de recerca concedides per la SCC aquest any 2021.
La SCC s’ha adherit al consens sobre la vacuna antipneumocòccica
La Societat Catalana de Cardiologia ha firmat, conjuntament amb altres societats científiques espanyoles, el document de consens recomanant la vacuna antipneumocòccica i sol·licita la inclusió de VPC13 per persones adultes, tant per edat (a partir dels 65 anys), com per malalties de risc a tot adult (incloent-hi les malalties cròniques), en el programa de vacunació vigent a Catalunya. Malgrat que les Societats Científiques signants del present document aplaudeixen que la Conselleria de Salut en el Calendari Vacunal Infantil hagi inclòs la VPC13 per tots els nens nascuts a partir de l'1 de gener de 201635, considerant que Catalunya hauria de fer un pas endavant per equiparar-se a altres Comunitats Autònomes i a altres països de l’entorn, finançat VPC13 per totes les persones ≥65 anys, independentment de la seva condició clínica, i per les persones ≥50 anys amb malalties cròniques de risc.
AMPLIACIÓ de TERMINI - Oberta la convocatòria de beques de la Societat Catalana de Cardiologia 2021
El nou termini de presentació de sol·licituds acaba el dia 6 d’abril de 2021 a les 23:59 hores. S’han convocat dues beques per a projectes de recerca originals i inèdits. Cada beca està dotada amb 10.000 € més 1.000 € addicionals si el treball és acceptat per ser publicat en una revista amb Impact Factor. La data límit de recepció de les memòries és el 30 de març de 2021.
La Intel·ligència Artificial i el Big Data demostren la seva eficàcia en la detecció precoç de la hipercolesterolèmia familiar i insuficiència cardíaca
Dos nous estudis presentats a l’e-Congrés SEC de la salut cardiovascular revelen noves dades
El tractament de base amb estatines millora el pronòstic en pacients ingressats per COVID-19
Un estudi amb dades de 19 hospitals catalans revela una mortalitat entre un 22% i un 25% menor en pacients en teràpia amb estatines
Un estudi demostra el potencial d'utilitzar drons per al lliurament de DEA en cas d’una aturada cardíaca
El 90% de persones que experimenten una aturada cardíaca no sobreviuen a l'episodi
L’Hospital Clínic avalua l’eficàcia de l’oclusió de l’orelleta esquerra com a alternativa als anticoagulants en la fibril·lació auricular
El Clínic participa en l’estudi CATALYST, que compara la teràpia anticoagulant amb el tancament de l’orelleta esquerra en pacients amb fibril·lació auricular no valvular
Selfies per a detectar malalties cardiovasculars
Un algoritme informàtic detecta la malaltia de les artèries coronàries a través de quatre fotos
Un esquema gràfic resumeix el maneig de la dislipèmia en prevenció secundària de la síndrome coronària aguda
Un treball gràfic presentat en el darrer Congrés de la Societat Catalana de Cardiologia (SCC) ofereix informació rellevant sobre el maneig de les dislipèmies en prevenció secundària en pacients amb síndrome coronària aguda. L’esquema recull les analítiques a realitzar, els objectius a assolir i les pautes de tractament al llarg de les diferents fases de seguiment.
Un algoritme del CNIC avisa del risc cardiovascular en persones sanes
Pot millorar la pràctica clínica de persones aparentment sanes i amb un baix risc cardiovascular segons els marcadors tradicionals
Les millors comunicacions presentades al 32 Congrés de la Societat Catalana de Cardiologia
En el marc del 32 Congrés de la Societat Catalana de Cardiologia es van atorgar tres premis a les millors comunicacions presentades. Es poden consultar els projectes guanyadors en l'enllaç de la notícia
La relació entre COVID-19 i les malalties cardiovasculars protagonitza les sessions científiques de l’AHA 2020
Les Scientific Sessions de l’AHA es van celebrar en format virtual del 13 al 17 de novembre. L’impacte de la COVID-19 i els resultats més recents d’assaigs clínics en diversos àmbits de la cardiologia van centrar un programa replet de propostes. Les diferents sessions són accessibles sota demanda per a usuaris registrats.
La ESC analitza el paper de la salut digital en cardiologia
La European Society of Cardiology (ESC) ha organitzat un event totalment online al voltant de la salut digital aplicada a la cardiologia. Durant una setmana, la ESC Digital Health Week ha analitzat les últimes actualitzacions digitals sobre dispositius i aplicacions mòbils; intel·ligència artificial (IA) i big data: i teleconsultes i monitorització remota.
Beca i Premis del Consell Català de Ressuscitació 2014
Obert el termini per la presentació de la Beca i Premis del Consell Català de Ressuscitació 2014
Nou format per les sessions de formació dels primers dilluns de mes de la Societat Catalana de Cardiologia
Les sessions d'actualització en cardiologia dels primers dilluns de mes, iniciades el 5 d'octubre, es realitzaran en format webinar. La primera sessió webinar del 5 d'octubre va ser un èxit amb més de 40 assistents on line. Consultar el programa complet en l'enllaç de la notícia
Guanyadors Beques Societat Catalana de Cardiologia 2020
Durant la clausura del 32 Congrés de la Societat es van anunciar els guanyadors de les beques SCC 2020. Es poden consultar els projectes guanyadors en l'enllaç de la notícia
La Societat Catalana de Cardiologia ha convocat una BECA DE COMUNICACIÓ
La SCC atorga una beca per un soci de la SCC que dugui a terme un projecte d’estudi i de col·laboració en la difusió d’imatge i informació de la Societat cap als socis, els professionals, els mitjans i la ciutadania. El termini de presentació és el 30 de juny, consultar les bases en l'enllaç de la notícia
32 Congrés de la Societat Catalana de Cardiologia
S'ha cancel.lat el congrés previst pels dies 4 i 5 de juny a la Universitat de Barcelona i es celebrará en format virtual, on line, els dies 16, 17 i 18 de setembre del 2020.
Comunicat sobre inici del tractament anticoagulant en els pacients amb fibril·lació auricular en el context de l'emergència sanitària COVID-19
Es pot consultar el comunicat complet en l'enllaç de la notícia.
Resolució del 5 de març de 2020 de la Hble. Consellera de Salut, per la qual s’adopten les mesures de caire organitzatiu per a la prevenció i el control de la infecció pel SARS-CoV-2 en el col·lectiu dels professionals sanitaris.
Es pot consultar el comunicat complet en l'enllaç de la notícia
Convocatòria beques Daniel Bravo 2020
La Fundació Privada Daniel Bravo Andreu obre la convocatòria 2020 de les beques per a estades curtes d’investigació biomèdica a l’estranger amb l’objectiu principal d’estimular la recerca d’alt impacte a Catalunya. La convocatòria romandrà oberta fins l’11 de març de 2020. Es pot consultar l'estat a l'enllaç de la notícia
S'inicien les sessions d'Actualització en Cardiologia dels dilluns de la SCC amb gran assistència
Maneig de la insuficiència cardíaca aguda per valvulopatia el 2019, va ser la primera sessió del curs 2019-20
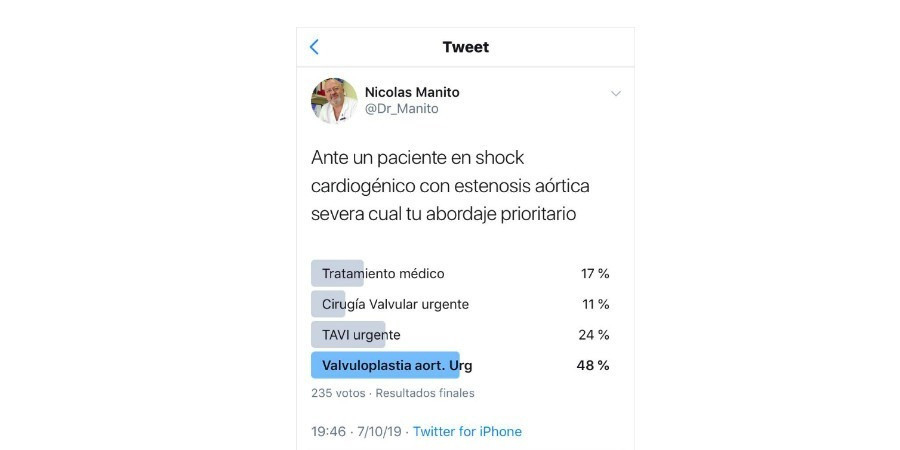
Consulteu aquí el resultat de l'enquesta que es va realitzar durant la primera sessió del curs d'Actualització en Cardiologia del curs 2019-20
Davant un pacient en xoc cardiogènic amb estenosi aòrtica severa, quin és l'abordatge prioritari? Resposta en la imatge de la notícia.
“Les pacients, la societat i el sistema sanitari minimitzen el risc cardiovascular de les dones”
Entrevista amb la Dra. Paola Beltran, responsable del Servei de Cardiologia de l’Hospital de Viladecans i coordinadora del Projecte post-IAM Catalunya, del Departament de Salut
Guanyadors de les Beques SCC 2019
Durant el 31è Congrés de la SCC, es va fer públic els guanyadors de la convocatòria de beques 2019
7 de juny, conferència del Dr. Valentín Fuster en el marc del 31è Congrés de la Societat Catalana de Cardiologia
El Repte Científic #1: entenent i promovent la salut cardiovascular des de la infància al llarg de tota la vida.
PROGRAMA 31è CONGRÉS DE LA SOCIETAT CATALANA DE CARDIOLOGIA
Ja està disponible el programa del 31è congrés de la Societat Catalana de Cardiologia.
Novetat al Congrés SCC 2019: espai tecnològic-startups en Cardiologia
El Congrés de la SCC, incorpora com a novetat a l’edició del 6 i 7 juny, un “espai tecnològic-startups en Cardiologia”, on es facilitarà que projectes innovadors es puguin donar a conèixer en petites càpsules de 5 minuts d’exposició. Els interessats en participar-hi poden contactar amb la Societat: sccardiologia@academia.cat
Convocatòria beques Societat Catalana de Cardiologia 2019
Es convoquen dues beques per a projectes de recerca originals i inèdits.
Convocatòria beques Daniel Bravo 2019
la Fundació Privada Daniel Bravo Andreu ha obert la convocatòria per a estades curtes a l’estranger en investigació cardiovascular. La convocatòria romandrà oberta del 30 de gener al 6 de març de 2019, i l’estada s’iniciarà entre l’1 de maig i el 30 de novembre de 2019.
Us fem saber que s’ha obert el termini per la presentació de la Beca i Premis del Consell Català de Ressuscitació 2019.
Beca per un projecte de recerca 2019 Premi a la millor publicació en revista científica 2019 Premi a la millor Tesi doctoral 2019 Premi a la millor comunicació 2019
Més de 1000 inscrits al 30è Congrés de la Societat Catalan de Cardiologia.
L’última edició del Congrés de la SCC que es va celebrar el passat 31 de maig i 1 de juny a la Universitat de Barcelona, es va tancar amb 1053 inscrits.
Guanyadors de les Beques SCC 2018
Durant el 30è Congrés de la SCC, es va fer públic els guanyadors de la convocatòria de beques 2018
La Societat Catalana de Cardiologia concedirà el seu premi anual “Joan Codina Altés” al Director de l’entitat Proactiva Open Arms, l'Òscar Camps.
La Societat Catalana de Cardiologia concedirà aquest 2018 el guardó anual “Joan Codina Altés” al director de Proactiva Open Arms, l'Òscar Camps, en reconeixement a la seva tasca humanitària.
Setmana de la Insuficíencia Cardíaca (7-13 maig 2018) a nivell mundial
"Mou-te per la insuficiència cardiaca" va ser un acte per la setmana de conscienciació sobre la insuficiència cardiaca on va participar el GICCAT.
La Societat Catalana de Cardiologia ha convocat eleccions per a la renovació parcial de la Junta Directiva.
A partir de l’11 d’abril 2018, s’obre el període d’enviament de candidatures.
Calendari eleccions de renovació parcial de la Junta Directiva per al període 2018-19
Calendari eleccions de renovació parcial de la Junta Directiva de la SCC.
El 27 de febrer es presenta la formació de formadors: Atenció a la síndrome coronària Aguda i l'abordatge dels pacient POST-IAM a L'Auditori CAMFIC
La Directora del Pla Director de Malalties Cardiovasculars, presentarà el document: Model de rehabilitació cardíaca i prevenció secundària en persones que han tingut una síndrome coronària aguda.
Beques Daniel Bravo per a estades curtes a l'estranger en investigació cardiovascular
S'ha obert la convocatòria 2018 de les Beques Daniel Bravo per a estades curtes a l'estranger d'investigació cardiovascular fins el 15 de març.
S'ha obert la convocatòria 2018 de Beques de la Societat Catalana de Cardiologia
Ja es poden consultar les bases de la convocatòria de beques 2018 al següent enllaç: : http://www.catcardio.cat/?p=page/html/beques
Oberta la convocatòria de beques i premis de l'Acadèmia del curs 2017-2018
Data límit de presentació 6 de febrer 2018
Oberta la convocatòria de Beques i Premis del Consell Català de Ressuscitació 2018.
Beca per un projecte de recerca 2018 Premi a la millor publicació en revista científica 2018 Premi a la millor comunicació 2018
Claus per aconseguir una pràctica esportiva amb menys risc
El Grupo de Trabajo de Cardiología del Deporte de la Sociedad Española de Cardiología (SEC) va participar en el II Congreso Nacional contra la Muerte Súbita en el deporte, abordant amb detall les claus per aconseguir una pràctica esportiva amb menys riscos.
S'ha obert la convocatòria 2017 de les Beques de la Societat Catalana de Cardiologia
Ja es poden consultar les bases de la convocatòria de beques 2017 al següent enllaç: http://www.catcardio.cat/?p=page/html/beques
Beca i Premis del Consell Català de Ressuscitació 2017.
Obert el termini per la presentació de la Beca i Premis del Consell Català de Ressuscitació 2017.
Dia mundial del Cor - Bateguem amb tu
El dia 29 de setembre celebrem a les Cotxeres Borbó el Dia Mundial del Cor
Curs de formació continuada: Processos Compartits entre Atenció Primària i Cardiologia
S'han obert les inscripcions on-line
I Jornada d'Actualització. Grup d'Unitats de Cures Agudes Cardiològiques
S'han obert les inscripcions on-line
Acord entre la Societat Catalana de Cardiologia i la Societat Catalana de Medicina Familiar i Comunitària
El passat dilluns 20 de juny es va du a terme la signatura de l’acord de creació del Grup de Treball de la SCC i de la Camfic per a la coordinació entre Cardiologia i Atenció Primària.
Grup de Treball d'Insuficiència Cardìaca
Recentment s'ha reconstituït el grup de treball d'Insuficiència Cardìaca de la Societat Catalana de Cardiologia (GICCAT)
Grup de treball de la Societat Catalana de Cardiologia per a la coordinació entre Cardiologia i Atenció Primària
S'ha creat el grup de treball de la Societat Catalana de Cardiologia per a la coordinació entre Cardiologia i Atenció Primària
Convocatòria d'eleccions per a la renovació parcial de la Junta Directiva de la SCC
A partir del 13 d’abril 2016, s’obre el període d’enviament de candidatures.
Beques Daniel Bravo per a estades curtes a l'estranger d'investigació biomèdica
S'ha obert la convocatòria 2016 de les Beques Daniel Bravo per a estades curtes a l'estranger d'investigació biomèdica.
Grup de treball de Cures Agudes Cardiològiques
S'ha creat el grup de treball de Cures Agudes Cardiològiques dins la Societat Catalana de Cardiologia
Beques Societat Catalana de Cardiologia 2016
Ja es poden consultar les bases de la convocatòria de beques 2016 en : http://www.catcardio.cat/beques.php
1ª Convocatòria anual (2016) d’accés a les dades del Registre del Codi IAM
El Comitè Científic del codi IAM realitza dues convocatòries anuals per a poder accedir a la base de dades del registre del codi.
Beca i Premis del Consell Català de Ressuscitació 2016.
En el següent enllaç trobaran les bases i impresos de sol.licitud.
Nova recomanació del projecte Essencial (octubre 2015)
Antagonistes de canals de calci després d'un infart de miocardi. En pacients després d’un infart de miocardi no es recomana la prescripció rutinària d’antagonistes del canal de calci per reduir el risc cardiovascular.
28 Congrés de la Societat Catalana de Cardiologia 2016
El 28 Congrés de la Societat, es celebrarà els dies 2 i 3 de juny de 2016 a l'Institut d'Estudis Catalans - c/ del Carme, 47 - Barcelona
Grup de Treball de Rehabilitació Cardíaca i Prevenció Secundària
S'ha creat el Grup de Treball de Rehabilitació Cardíaca i Prevenció Secundària dins de la Societat Catalana de Cardiologia
Inhibidors de l'adenosina difosfat en pacients amb síndrome coronària aguda sense elevació del segment ST
En l’apartat “Documentació” es pot consultar aquest l'informe.
Informació del congrés celebrat els dies 4 i 5 de juny de 2015
Es pot consultar informació del XXVII Congrés celebrat els dies 4 i 5 de juny de 2015
Projecte ESSENCIAL
Essencial promou recomanacions per evitar pràctiques clíniques de poc valor. NOVETAT: AINE en malaltia cardiovascular, renal crònica o insuficiència hepàtica.
Beques Daniel Bravo
S'ha hobert la convocatòria 2015 de les Beques Daniel Bravo per a estades curtes a l'estranger d'investigació biomèdica.
Beques Societat Catalana de Cardiologia 2015
Ja es poden consultar les bases de la convocatòria de beques 2015 en : http://www.catcardio.cat/hbeques.php
Convocatòria de Projectes Daniel Bravo de recerca en pediatria
La Fundació Privada Daniel Bravo Andreu ha posat en marxa la primera convocatòria de Projectes Daniel Bravo de recerca en pediatria.
Beca i Premis del Consell Català de Ressuscitació 2015
Obert el termini per la presentació de la Beca i Premis del Consell Català de Ressuscitació 2015
Projecte ESSENCIAL
Recomanacions publicades amb l'objectiu de millorar la qualitat de la pràctica clínica. Nova recomanació (gener 2015)
Ordenació i configuració del model organitzatiu dels serveis de cirurgia cardíaca
Pla d'acció de cirurgia cardíaca (PACC)
Beques Fundació Daniel Bravo-Andreu
Beques Fundació Daniel Bravo-Andreu per a estades curtes a l'estranger
Informació eleccions Junta Directiva
Eleccions de renovació parcial de la Junta Directiva per al període 2014-2015
Reglament per l'elecció parcial de la Junta Directiva de la Societat Catalana de Cardiologia
Reglament per l'elecció de la Junta Directiva de la SCC.
Calendari eleccions de renovació parcial de la Junta Directiva per al període 2014-15
Calendari eleccions de renovació de la Junta Directiva de la SCC.
Data límit recepció de les memòries de les Beques de la Societat Catalana de Cardiologia 2014
Beques per a projectes de recerca de la SCC 2014
Data límit per enviar comunicacions al XXVI Congrés de la Societat Catalana de Cardiologia
XXVI Congrés de la Societat Catalana de Cardiologia, dies 29 i 30 de maig de 2014
Socis estratègics de la societat






Socis col·laboradors